CHEMIA
KWASY
KARBOKSYLOWE
Kwasy karboksylowe to związki organiczne o wzorze ogólnym R-COOH,
przy czym –COOH to grupa karboksylowa, a R-COO to reszta kwasowa. Dysocjują w
wodzie, w reakcji z wodorotlenkami tworzą sole, z alkoholami i fenolami –
estry. Szeroko rozpowszechnione w przyrodzie.
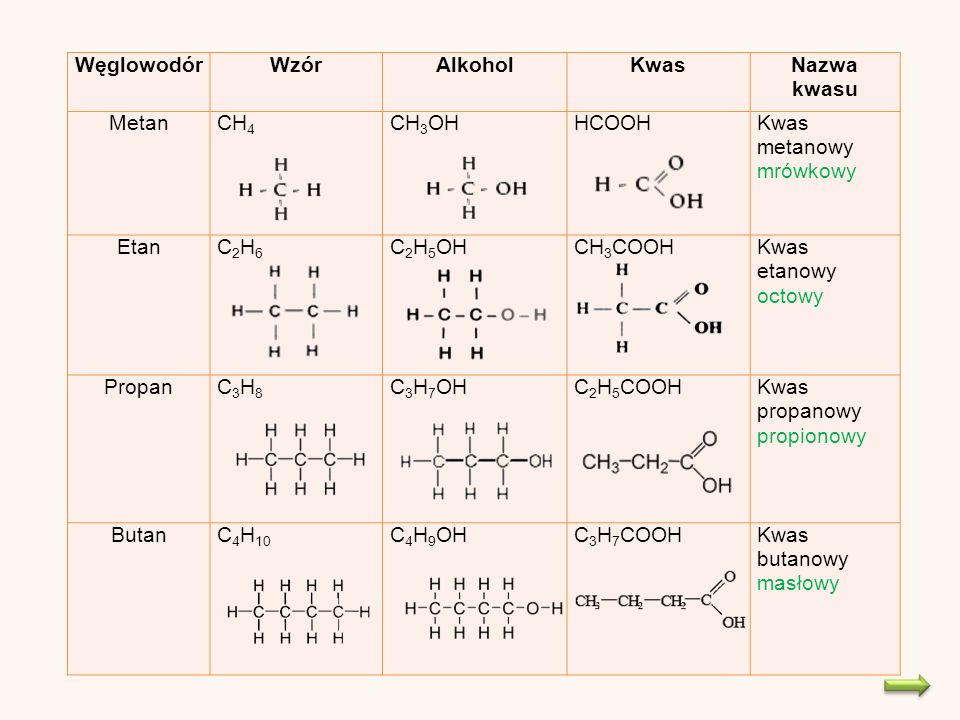
Przykładowe kwasy karboksylowe:
FERMENTACJA OCTOWA
Kwas otrzymywany jest katalitycznie z acetylenu (przez aldehyd octowy jako półprodukt), jako produkt uboczny suchej destylacji drewna lub utleniania alkoholu etylowego.
W roztworach zawierających alkohol etylowy, np. w winie, pod wpływem odpowiednich gatunków bakterii i wydzielanych przez nie enzymów następuje powolne utlenianie.
Proces ten nazywa się fermentacją octową. Otrzymany wodny roztwór kwasu octowego to powszechnie znany ocet. W zależności od surowca poddanego fermentacji rozróżnia się ocet winny (6% kwasu), spirytusowy (10% kwasu), piwny i inne. Kwas octowy w postaci octu jest stosowany w przemyśle spożywczym i w gospodarstwie domowym jako środek konserwujący i przyprawa.
Kwas otrzymywany jest katalitycznie z acetylenu (przez aldehyd octowy jako półprodukt), jako produkt uboczny suchej destylacji drewna lub utleniania alkoholu etylowego.
W roztworach zawierających alkohol etylowy, np. w winie, pod wpływem odpowiednich gatunków bakterii i wydzielanych przez nie enzymów następuje powolne utlenianie.
Proces ten nazywa się fermentacją octową. Otrzymany wodny roztwór kwasu octowego to powszechnie znany ocet. W zależności od surowca poddanego fermentacji rozróżnia się ocet winny (6% kwasu), spirytusowy (10% kwasu), piwny i inne. Kwas octowy w postaci octu jest stosowany w przemyśle spożywczym i w gospodarstwie domowym jako środek konserwujący i przyprawa.
ZASTOSOWANIE KWASÓW KARBOKSYLOWYCH
Jednym z ważniejszych zastosowań kwasów karboksylowych są mydła. Są one mieszaniną soli sodowych wyższych kwasów karboksylowych z dodatkami substancji zapachowych, barwnych i ułatwiających formatowanie. Mydła można otrzymywać na różne sposoby, między innymi w reakcji kwasu z wodorotlenkiem.
Kwas stearynowy podczas ogrzewania reaguje z wodorotlenkiem sodu powoli, według równania:
CH3—(CH2)16— COOH +NaOH® CH3—(CH2)16—COONa + H2O
Powstający stearynian pieni się w sposób typowy dla mydła.
Solami najczęściej wykorzystywanymi w mydłach są:
-palmitynian sodu CH3 –(CH2)14 –COONa
-stearynian potasu CH1 –(CH2)16 –COOK
Innymi sposobami na wykorzystanie kwasów karboksylowych jest:
-konserwacja przetworów owocowych i warzywnych (benzoesan sodu)
-kwas octowy w różnych formach (ocet-10%, esencja octowa-80%, lodowaty-czysty)
-tłuszcze oraz oleje roślinne(glicerydy)- powstają w reakcji kwasów tłuszczowych z gliceryną.
Jednym z ważniejszych zastosowań kwasów karboksylowych są mydła. Są one mieszaniną soli sodowych wyższych kwasów karboksylowych z dodatkami substancji zapachowych, barwnych i ułatwiających formatowanie. Mydła można otrzymywać na różne sposoby, między innymi w reakcji kwasu z wodorotlenkiem.
Kwas stearynowy podczas ogrzewania reaguje z wodorotlenkiem sodu powoli, według równania:
CH3—(CH2)16— COOH +NaOH® CH3—(CH2)16—COONa + H2O
Powstający stearynian pieni się w sposób typowy dla mydła.
Solami najczęściej wykorzystywanymi w mydłach są:
-palmitynian sodu CH3 –(CH2)14 –COONa
-stearynian potasu CH1 –(CH2)16 –COOK
Innymi sposobami na wykorzystanie kwasów karboksylowych jest:
-konserwacja przetworów owocowych i warzywnych (benzoesan sodu)
-kwas octowy w różnych formach (ocet-10%, esencja octowa-80%, lodowaty-czysty)
-tłuszcze oraz oleje roślinne(glicerydy)- powstają w reakcji kwasów tłuszczowych z gliceryną.
WŁAŚCIWOŚCI FIZYCZNE KWASÓW
KARBOKSYLOWYCH
Kwasy karboksylowe dzielimy
na niższe i wyższe (kw. tłuszczowe)
Kwasy karboksylowe niższe
to:
-kw. mrówkowy HCOOH;
składnik jadu mrówek, pszczół i pokrzyw; grupa R-wodór
-kw. octowy CH3COOH;
powstaje w roztworach zawierających alkohol etylowy; grupa R-metyl
Kwasy tłuszczowe to takie, w
których grupa R zawiera długi łańcuch węglowy, między innymi:
-kw. palmitynowy CH3
–(CH2)14 –COOH
-kw. stearynowy CH3 –(CH2)16
–COOH
-kw. oleinowy
Długość łańcucha węglowego
ma swoje następstwa przy właściwościach fizycznych. Kwasy, które w grupie R
mają tylko kilka atomów węgla są bezbarwnymi cieczami. Jednak wraz ze wzrostem
atomów tego pierwiastka ciecz staje się bardziej oleista, aż występuje jako
ciało stałe. Także rozpuszczalność w wodzie jest od tego zależna. Kwasy zawierające
do 3 atomów węgla mieszają się z tą cieczą w każdym stosunku, natomiast te,
które posiadają 7 lub więcej- są prawie nierozpuszczalne. Prócz tego jest lotny
i higroskopijny.
WŁAŚCIWOŚCI CHEMICZNE KWASÓW KARBOKSYLOWYCH
Kwasy karboksylowe są na
ogół kwasami słabymi. Kwas mrówkowy i kwasy karboksylowe zawierające w grupie
węglowodorowej kilka atomów węgla są bezbarwne i posiadają indywidualny ostry
zapach. Wykazują również zróżnicowaną rozpuszczalność w wodzie:
-kwasy zawierające do 3
atomów w grupie R mieszają się z wodą w każdym stosunku
-zawierające od 4 do 6
atomów węgla rozpuszczają kilka gramów na 100g wody
-zawierające 7 i więcej
atomów węgla są nierozpuszczalne w wodzie
Wodne roztwory kwasów
karboksylowych barwią lakmus i papierek uniwersalny na czerwono, czyli tak, jak
kwasy nieorganiczne. Są związkami bardzo reaktywnymi. Reagując z wodorotlenkami
tworzą sole, a z alkoholami i fenolami – estry. Ulegają dysocjacji, wytwarzając
jony H+. Dysocjacja kwasów karboksylowych przebiega według schematu:
R-COOH --> R-COO+ H+
Na przykład:
CH3–COOH --> CH3-COO+H+
Właściwości chemiczne kwasów
karboksylowych
-Palne
-Zapach ostry, intensywny
-Smak kwaśny
-Trujące działanie na
organizmy żywe żrące, wywołują oparzenia i podrażnienia
-Reaktywne
-Dysocjują
-Barwią lakmus/kolor tak / czerwony
Komentarze
Prześlij komentarz